当埃博拉病毒肆虐西非,感染者的器官与组织出血不止并在剧烈疼痛中死去时;当看到红丝带,让人联想到那可怕的至今已夺去数十万人生命的艾滋病毒时;当曝光某野生动物成为人类餐桌上的新宠,使我们担忧的想到因为捕食果子狸而爆发的“非典型肺炎”时;当禽流感爆发,大量的家禽被捕杀时,我们不禁要问,哪里来的这么多的病毒?在医学发达的今天,病毒何以如此可怕?面对病毒,我们该怎样回击?
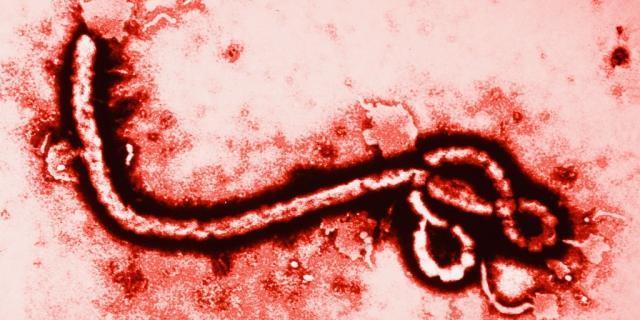
若要弄清楚以上几个问题,需要对病毒进行全面的剖析。作为世界上最小的生物,病毒要比细菌还小百倍。所以狡猾的病毒能通过除菌滤器。只有借助电子显微镜才能看见。病毒的结构非常简单,大多数病毒只是一团由蛋白壳体做“外衣”包裹着基因物质的核壳体而已。但因此也产生了病毒的两个“鲜明的特色”:一般生物细胞中的核酸均含有DNA与RNA这两种遗传物质,但是病毒却只拥有其中的一种,如乙肝病毒内的核心部分为双链DNA,而艾滋病毒内部的遗传密码却是分布在RNA分子上,更为奇特的是引起疯牛病的朊病毒居然只是蛋白质分子,不含任何遗传物质;另外,病毒的内部结构虽然极为简单,但外部形态却有很多种。如乙肝病毒与艾滋病毒均为颗粒状;埃博拉病毒属于丝状病毒;SARS病毒则是一种冠状病毒的变种。
也正是因为病毒的结构极为简单,据此,一些科学家猜想,病毒可能是从普通细胞中“逃逸人体”出来的DNA或RNA片断,在获得了一些蛋白质或是部分细胞膜作为它们的外壳后而成为了独立的生命体病毒。如果这种猜想是真实的话,那么就意味着病毒这种古老的生物自20亿年前细胞最早出现后,就一直在地球上作乱。
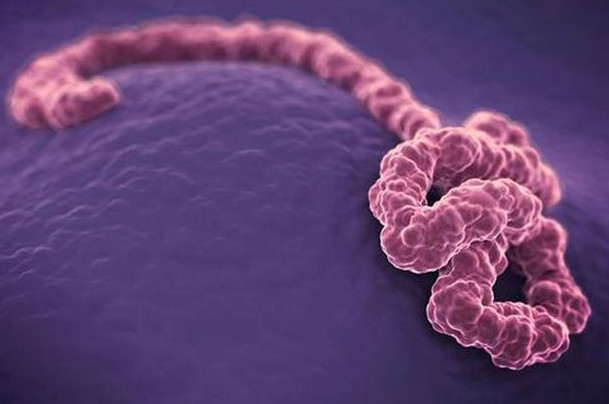
事实上,确实是从史前时代起,人类就遭遇到过病毒的侵害。除鼠疫、天花、牛痘等在人类历史上曾经有过“横扫世界”的强进势头并且造成重大损失的传统病毒外,最近几十年新的病毒正以一种令人胆颤的神秘方式不断出现。尤其是其中的大多数属于尚不为人所知的热带地方性病毒。目前,地球上大约有4000多种病毒,其中大约有100多种与人类疾病密切相关。其中的新兴病毒已经在人类全球健康网络上打开了缺口。比如,震惊全世界、至今无药可治的艾滋病毒;目前正在西非蔓延同样没有有效治愈方式,同时致死率又极高的埃博拉病毒;由蚊子携带并且可以随着气候变化的美国西尼罗河病毒等等。
这些“新兴病毒”本是长期隐藏于密林之中的,作为病毒的自然宿主,各种野生动物是一个巨大的天然病毒库。然而,多年来带有病毒的野生动物们一直未发生明显的症状。它们安安静静的潜伏不动,也可以说是在蛰伏待机。一旦生存环境发生改变,这些病原体就会抓住机会,得以转移到新的宿主或产生突变体,从而引发新的疾病,进而扩大种群。
在病毒传播的过程当中,地球的主宰——人类,同样扮演了“重要的”角色。当现代文明的发展使野生动物的栖息地遭到大面积破坏以后,动物们不得不向人类生活的区域转移;另一方面,随着交通工具与科学技术的发展,我们的足迹已几乎遍布世界各个角落,这也增加了人类与携带病毒的野生动物接触的机会。所以,新病毒的陆续出现大概也是人类破坏环境所付出的惨痛代价吧。
以埃博拉病毒为例,它并不是第一次出现在人类的视野之中,早在1976年就首次被发现于扎伊尔的埃博拉地区并因此而得名。据世界卫生组织(WHO)的统计,当时被感染的300名患者中,共有274人被病毒夺去了生命。没有有效的治疗与防治方法,几十年来,埃博拉病毒在非洲引起了数次发热和严重内出血的爆发流行,绝大多数的感染者难免死亡。
这种可怕的病毒爆发的原因,就始于人们处理受感染的肉类或者野生动物,特别是大型猿类动物。尽管人们还不清楚这些动物是如何传染这种病毒的。但不幸的是野生动物的肉却是这一地区居民主要的蛋白质来源。可是,病毒到底是如何从宿主身上转移到人类体内的呢?病毒的感染机制依然和它的核壳体结构相关。病毒需要寄生于活的宿主细胞,原因就在于病毒缺乏增殖所需要的酶系统,因此必须依赖于寄主细胞提供自我复制过程中所需要的原料体系、能量和场所。外部条件准备就绪后,病毒需要完成以下六个步骤完成其增殖活动,分别是吸附、侵入、脱壳、生物合成、组装和释放。
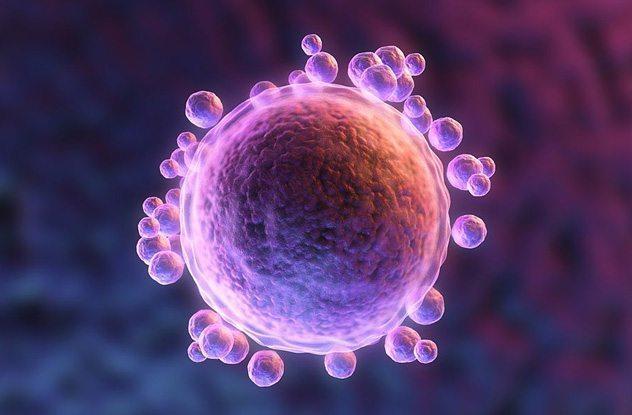
吸附作为这邪恶过程的第一步是决定感染成功与否的关键环节。现已发现,在吸附过程中,细菌的细胞壁以及动物细胞膜上的一种脂蛋白或糖蛋白充当了“内鬼”的角色。作为细胞表面受体,它们会与动物病毒或和噬菌体表面特异性的吸附蛋白发生相互作用而完成病毒的吸附过程;迄今为止,尚未发现植物细胞上有特异性的受体。
吸附的整个过程可在几分钟到几十分钟的时间内完成。成功附着到宿主细胞以后,病毒要么通过某种方式进入宿主细胞,要么会将含有复制病毒指令的基因物质注入宿主细胞之内。若病毒需要进入宿主细胞,简单来说,可以有四种方式:注射式侵入、细胞内吞、膜融合以及其他特殊的侵入方式。
有尾噬菌体可以通过尾部收缩将衣壳内的基因注入宿主细胞内,这样的方式称为注射式侵入;而动物病毒的常见侵入方式则是通过细胞内吞来完成。细胞膜内陷形成吞噬泡,病毒粒子从而得以进入细胞质当中;若病毒含有包膜,那么在侵入过程中,病毒包膜可以与细胞膜融合,最终使病毒得以进入细胞。若是植物病毒那么可以通过存在于植物细胞壁上的小伤口或天然的外壁孔侵入。植物细胞之间的胞间连丝也可以成为病毒入侵细胞的通道。正可谓是“条条大路通罗马”,根据病毒的种类不同,被侵入细胞的类型不同,病毒入侵细胞的方式可以是多种多样的。
完成入侵步骤以后,病毒在细胞内将会首先发生脱壳过程。这是指病毒感染性核酸从衣壳内被释放出来的过程。无包膜病毒只需要脱衣壳;有包膜的病毒,脱壳过程包括脱包膜和脱衣壳这两个步骤,方式因“病毒”而异。紧接着病毒会“马不停蹄”的进行生物合成。即根据基因指令,并借助宿主细胞提供的原料、能量和场所来合成核酸和蛋白质。
这是病毒基因组进行复制和表达的一个过程。以病毒核酸为模板在酶的作用下合成新的核酸分子,并以病毒RNA或病毒DNA的转录产物作为信使RNA,在细胞的核糖核蛋白体上合成衣壳蛋白,此过程中所需要的多数酶也来自宿主细胞。而在此阶段,胞浆中并没有病毒颗粒,因此被称为隐蔽期。
病毒的结构成分,核酸和蛋白质已分别准备就绪,随后在细胞核内或细胞质内发生装配过程,即组装成核衣壳。绝大多数DNA病毒是在细胞核内组装,而RNA病毒与痘病毒类则在细胞质内组装。无包膜病毒组装成核衣壳以后即成为成熟的病毒体。最后即是释放过程,也是在此过程中,绝大多数有包膜病毒通过细胞内的内质网、空泡,或以出芽方式释放而成为成熟病毒。在这一系列的过程当中对细胞膜破坏较轻,宿主细胞死亡慢;而无包膜病毒释放时被感染的细胞崩解,释放出病毒颗粒。宿主细胞膜被破坏,细胞也随即死亡。
从单个病毒吸附开始至病毒释放完成,整个过程称为感染周期。并且鉴于病毒是严格的细胞内寄生生物,又没有独立的代谢系统,很难找到杀死病毒而不伤害寄主的处理手段和药物。因此防重于治是对付病毒的基本方针。预防病毒的主要措施有:消灭传染源、铲除传染媒介、接种疫苗也是一个有效措施。消灭传染源这是预防动、植物和微生物病毒的有效措施,包括卫生检疫、隔离、铲除传染源;另外动植物病毒大都通过媒介传染,以昆虫为主。
例如乙型脑炎通过蚊子传染、许多植物病毒通过蚜虫传播。因此消灭传染媒介对于病毒的预防显得更为重要;虽然病毒的复制速度极快,杀伤力极大,但是也不可以为所欲为依然会遭遇“强敌”,即生物免疫系统——分为特异性免疫和非特异性免疫。到处“巡视”的淋巴细胞随时准备消灭外来入侵物质,一旦受到抗原刺激就会启动人体特异性免疫,产生大量的抗体与抗原相抗衡。接种疫苗就是利用了特异性免疫学原理。在遭遇病毒的大规模袭击前,有意给人体注入病毒的蛋白壳体(即疫苗)可使人体免疫系统为病毒的大规模袭击做好准备。这种方法己经挽救了几百万人的生命。但是据上文介绍可知病毒的结构极其的简单,这便意味着它们能够迅速变异。
所以,在一种病毒爆发以后的很长一段时间内似乎消失了,但是不知哪天就会“重整旗鼓”以一个新面孔的形式“卷土重来”。又或者一种流感病毒疫苗不能彻底解决病毒性感冒一样。这是因为引起普通感冒的病毒通过不断改变蛋白壳体,使人类的免疫系统每次都需要对它们进行重新确认,从而为病毒在人群中传播赢得了时间。另一方面不需要抗体参加的抗病毒作用称为非特异性免疫,其中最重要的是干扰素,它是机体对抗病毒感染而产生的一种物质。直接使用干扰素或干扰素诱导剂都可有一定的防治效果。
人类与病毒的战争还在继续。但是在这个过程当中也存在很多值得我们反思的问题。保护野生动物栖息地,减少人类活动对野生动物造成的影响,就会减少我们与携带各种病毒的野生动物的接触,也就大大降低了“新兴病毒”出现的几率。人类的活动不仅对地球上的其他生物,甚至对人类自身已经造成伤害,人类与病毒的战争还在继续,人类思想与行动的战争依然在持续。










